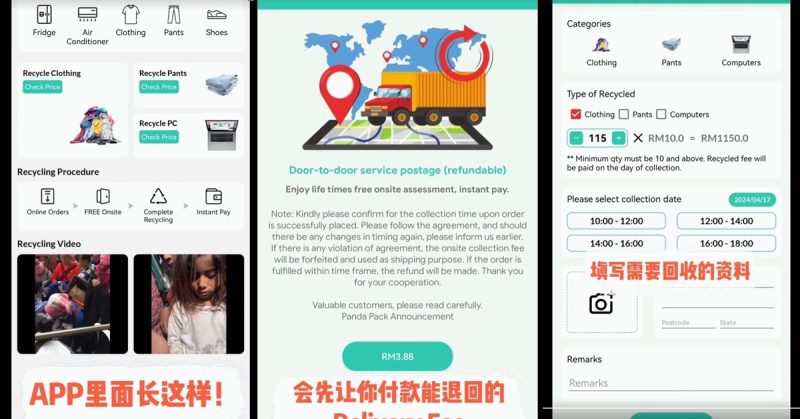
◤肺炎疫情◢科兴疫苗抵新但未采用 卫长:要考量很多因素
(新加坡28日讯)中国科兴新冠疫苗抵新,但还未获准使用引起讨论,疫苗须达到多少效能才会被批准,卫长解释是否批准不只看效能,还有其非常多考量。
ADVERTISEMENT
ADVERTISEMENT
《新明日报》报导,科兴疫苗2月初发表了第三阶段临床测试结果。数据显示,医护人员相隔14天接种两剂疫苗的保护效力为50.65%,对需要就医的病例保护效力为83.70%,对住院、重症及死亡病例的保护效力为100%。
新加坡目前获准使用辉瑞和莫德纳的冠病疫苗,效能都在90%以上,因此科兴疫苗是否会被我国批准引起关注。
卫生部兼通讯及新闻部高级政务部长普杰立医生日前深夜通过社交软体Clubhouse和网络媒体Zyrup成员交流,并欢迎听众发问。
在谈到疫苗效能不同但公众又不能选择施打哪一款,这是否会影响接种计划时,普杰立就说,除非新国现在有非常多疫苗可供选择,而且有非常大的数量,否则无法做到让公众能自选疫苗。
另外,谈到新国在核准疫苗方面,究竟要达到多高的效能才可接受,普杰立就说,评估疫苗不能单单看效能,还有非常多条件需要考量,例如安全性的细节数据等等。
伊丽莎白诺维娜医院传染病专科医生梁浩楠受访时说,理论上疫苗只要能达到至少五六成的效能就可以被批准,疫苗的生产过程还有使用的材料是否符合国际安全标准等等,这些都是同等重要的。
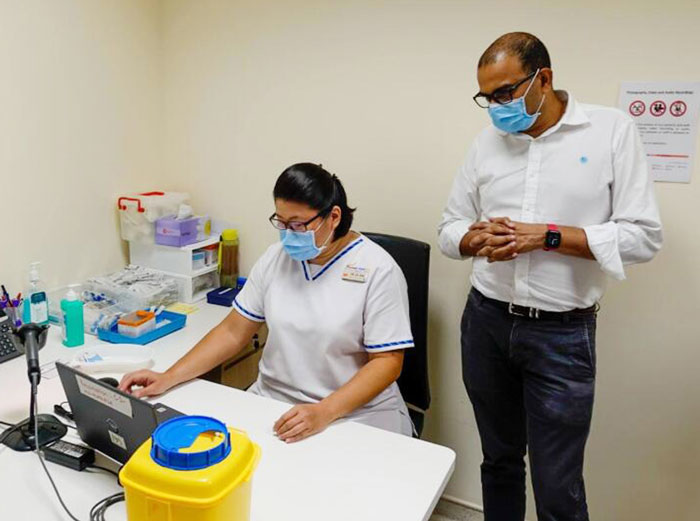
负责评估疫苗的卫生科学局医疗保健产品管理司司长曾清灵副教授接受《联合早报》的专访时说,由于还未收到科兴提供的完整数据,目前不便进一步评价该疫苗。
“他们使用的灭活病毒疫苗是一般人比较熟悉的科技,但这类疫苗有如流感疫苗一样,效能一般不会高于90%。”
他说,6道严格评估关卡中,首先是检查疫苗的化学配方(chemical formulation),看看是否存有杂质;第二道关卡是评估疫苗在动物的测试。设定这两个关卡,主要是为了确保不同剂量疫苗的化学成分,以及在动物身上的测试,是否达到符合安全的标准,才能进入临床测试。
“接下来必须跨过的三道关卡,则是疫苗的三期临床测试。”
他说,通过了这五道关卡后,生产商也须满足第六项要求:证明有良好生产规范(Good Manufacturing Practice,简称GMP),能安全且大规模地生产疫苗,才能获得批准。
他说,不同国家有不同的政策,一些欧美国家的药商一般会等到药物获得接收国批准后才开放出口。另外,除了科兴生物也有一些疫苗生产商正与卫生科学局接洽,但细节不便透露。
↓↓相关新闻↓↓
↓↓最近新闻↓↓